ヒトの新生児脳がもつ再生メカニズムを発見(新生児脳障害の再生医療の実現化に期待)
研究成果の概要
365体育投注大学院医学研究科の神農英雄助教(新生児?小児医学)、澤本和延教授(神経発達?再生医学)らの研究グループは、米国チルドレンズナショナル病院やペンシルバニア大学などとの国際共同研究により、ヒトの新生児がもつ脳障害後の神経再生メカニズムを世界で初めて明らかにしました。研究グループは、ヒト新生児の脳にのみ存在する神経幹細胞「外側放射状グリア」が脳障害後に活性化され、大脳白質のもとになるオリゴデンドロサイト前駆細胞の産生が増加することを発見しました。さらに、ヒト新生児と同様の脳構造をもつブタの実験により、外側放射状グリアを活性化させる薬剤を非侵襲的に投与することで、大脳白質傷害部のオリゴデンドロサイトの増加を促進し、白質の再生および運動機能の改善に成功しました。これらの知見により、新生児脳障害の再生医療の実現に大きく近づくことが期待されます。
研究のポイント
?新生児脳障害は重篤な後遺症を合併するため、新たな治療法の開発が望まれています。
?ヒト脳組織の解析により、ヒトの新生児脳に特徴的な神経幹細胞(注1)「外側放射状グリア(注2)」の細胞増殖能力が脳障害後に増強し、大脳白質のもとになるオリゴデンドロサイト前駆細胞(注3)の産生が増加することを初めて明らかにしました。
?網羅的遺伝子解析を通じて、細胞の増殖や生存に関わるATF5シグナル経路が外側放射状グリアの細胞増殖機能を調節することを解明しました。
?ヒト新生児と同様の脳構造をもつ新生仔ブタにATF5シグナル経路を活性化させる薬剤を経鼻投与し、傷害部での白質の再生と歩行機能の改善が促進しました。
?本研究の知見を発展させることで、新生児脳障害の再生医療の実現が期待できます。
?ヒト脳組織の解析により、ヒトの新生児脳に特徴的な神経幹細胞(注1)「外側放射状グリア(注2)」の細胞増殖能力が脳障害後に増強し、大脳白質のもとになるオリゴデンドロサイト前駆細胞(注3)の産生が増加することを初めて明らかにしました。
?網羅的遺伝子解析を通じて、細胞の増殖や生存に関わるATF5シグナル経路が外側放射状グリアの細胞増殖機能を調節することを解明しました。
?ヒト新生児と同様の脳構造をもつ新生仔ブタにATF5シグナル経路を活性化させる薬剤を経鼻投与し、傷害部での白質の再生と歩行機能の改善が促進しました。
?本研究の知見を発展させることで、新生児脳障害の再生医療の実現が期待できます。
背景
周産期医療が進歩した現在でも、低酸素や虚血による新生児脳障害は依然として年間数千例発生しています。大脳皮質と白質の両方が損傷を受けますが、白質障害は脳性麻痺などの重篤な神経学的後遺症を引き起こすため、社会的な問題になっています。傷害で失われた脳組織を再生させる治療法は無く、新たな治療法の開発が急務です。
生後の脳内でも脳室下帯という部分には神経幹細胞が存在し、大脳白質のもとになるオリゴデンドロサイト前駆細胞が産生されます。マウスを用いた研究では、脳障害後にオリゴデンドロサイト前駆細胞が傷害部へ移動することが知られています。このことから、脳室下帯の神経幹細胞は脳障害後の再生戦略に考慮されます。一方、ヒトの脳はマウスの脳と比べて、サイズや発達過程、脳室下帯の細胞構成などが大きく異なります。そのため、新生児脳障害の再生医療を実現するためには、ヒトの脳組織の解析が不可欠です。しかし、日本国内では倫理的な側面も含めてヒト脳組織の研究が非常に難しく、実際にヒトの脳障害後における神経再生能力については分かっていませんでした。
本研究では国際共同研究として、米国国立衛生研究所のニューロバイオバンクから提供されたヒト脳組織と、ヒト新生児と同様の脳構造を持つ新生仔ブタを実験に用いることにより、これらの解析を可能にしました。
生後の脳内でも脳室下帯という部分には神経幹細胞が存在し、大脳白質のもとになるオリゴデンドロサイト前駆細胞が産生されます。マウスを用いた研究では、脳障害後にオリゴデンドロサイト前駆細胞が傷害部へ移動することが知られています。このことから、脳室下帯の神経幹細胞は脳障害後の再生戦略に考慮されます。一方、ヒトの脳はマウスの脳と比べて、サイズや発達過程、脳室下帯の細胞構成などが大きく異なります。そのため、新生児脳障害の再生医療を実現するためには、ヒトの脳組織の解析が不可欠です。しかし、日本国内では倫理的な側面も含めてヒト脳組織の研究が非常に難しく、実際にヒトの脳障害後における神経再生能力については分かっていませんでした。
本研究では国際共同研究として、米国国立衛生研究所のニューロバイオバンクから提供されたヒト脳組織と、ヒト新生児と同様の脳構造を持つ新生仔ブタを実験に用いることにより、これらの解析を可能にしました。
研究の成果
まずヒトの脳の免疫組織学的解析を行ったところ、新生児の脳室下帯は成人より大きく、虚血性脳障害後にさらに拡大することが明らかになりました(図A)。その要因として、ヒトやブタのみに存在する神経幹細胞である外側放射状グリアの細胞増殖能力が増強されることを見出しました。さらに、新生児脳障害では、大脳白質のもとになるオリゴデンドロサイト前駆細胞の産生が増加することも発見しました。新生仔ブタの大脳白質虚血障害モデルでも同様の反応が再現され、脳室下帯で産生されたオリゴデンドロサイト前駆細胞が白質傷害部へ移動し、一部が分化することを明らかにしました(図B)。
次に、外側放射状グリアの増殖能力をコントロールするメカニズムを解明するため、網羅的遺伝子解析を行いました。その結果、細胞の増殖や生存を制御するATF5シグナルが、新生児脳障害後の外側放射状グリアで活性化されることを突き止めました。ATF5シグナルを阻害する薬剤(ソラフェニブ)を新生仔ブタに投与する実験の結果から、ATF5シグナルが外側放射状グリアの細胞増殖能力をコントロールすることを解明しました。
これらの結果を踏まえ、外側放射状グリアの細胞増殖能力が白質再生に寄与することを証明するため、ATF5シグナルを活性化させる薬剤(サルブリナール)を新生仔ブタに経鼻投与しました。サルブリナール投与により、脳障害がない場合でも外側放射状グリアの細胞増殖能力が増強されることがわかりました。さらに、脳障害後の新生仔ブタへサルブリナールを経鼻投与し、外側放射状グリアのATF5シグナルを持続的に活性化させたところ、脳室下帯から白質傷害部へ移動?分化したオリゴデンドロサイトの数が有意に増加しました。免疫組織学的解析や拡散テンソル画像解析(注4)から、傷害部における白質の密度や微細構造が回復したことを明らかにしました。また、歩行テストの結果、サルブリナールの経鼻投与によって脳障害後の新生仔ブタの歩行機能が有意に改善しました(図C)。
次に、外側放射状グリアの増殖能力をコントロールするメカニズムを解明するため、網羅的遺伝子解析を行いました。その結果、細胞の増殖や生存を制御するATF5シグナルが、新生児脳障害後の外側放射状グリアで活性化されることを突き止めました。ATF5シグナルを阻害する薬剤(ソラフェニブ)を新生仔ブタに投与する実験の結果から、ATF5シグナルが外側放射状グリアの細胞増殖能力をコントロールすることを解明しました。
これらの結果を踏まえ、外側放射状グリアの細胞増殖能力が白質再生に寄与することを証明するため、ATF5シグナルを活性化させる薬剤(サルブリナール)を新生仔ブタに経鼻投与しました。サルブリナール投与により、脳障害がない場合でも外側放射状グリアの細胞増殖能力が増強されることがわかりました。さらに、脳障害後の新生仔ブタへサルブリナールを経鼻投与し、外側放射状グリアのATF5シグナルを持続的に活性化させたところ、脳室下帯から白質傷害部へ移動?分化したオリゴデンドロサイトの数が有意に増加しました。免疫組織学的解析や拡散テンソル画像解析(注4)から、傷害部における白質の密度や微細構造が回復したことを明らかにしました。また、歩行テストの結果、サルブリナールの経鼻投与によって脳障害後の新生仔ブタの歩行機能が有意に改善しました(図C)。
研究の意義と今後の展開や社会的意義など
今回の研究成果は、ヒト新生児の脳に特有の神経再生メカニズムを世界で初めて解明したものです。ヒトの脳組織を解析したことで、これまで機能が不明であった生後の外側放射状グリアが重要な役割を持つことも明らかにしました。また、本研究では非侵襲的な手法を用いた脳障害の再生方法を示しており、新生児脳障害の治療法として実現可能性が高いことが期待できます。本研究の知見を発展させることで、新生児脳障害の再生医療の進展につながり、こどもたちの未来を守る大きな一歩になると考えられます。
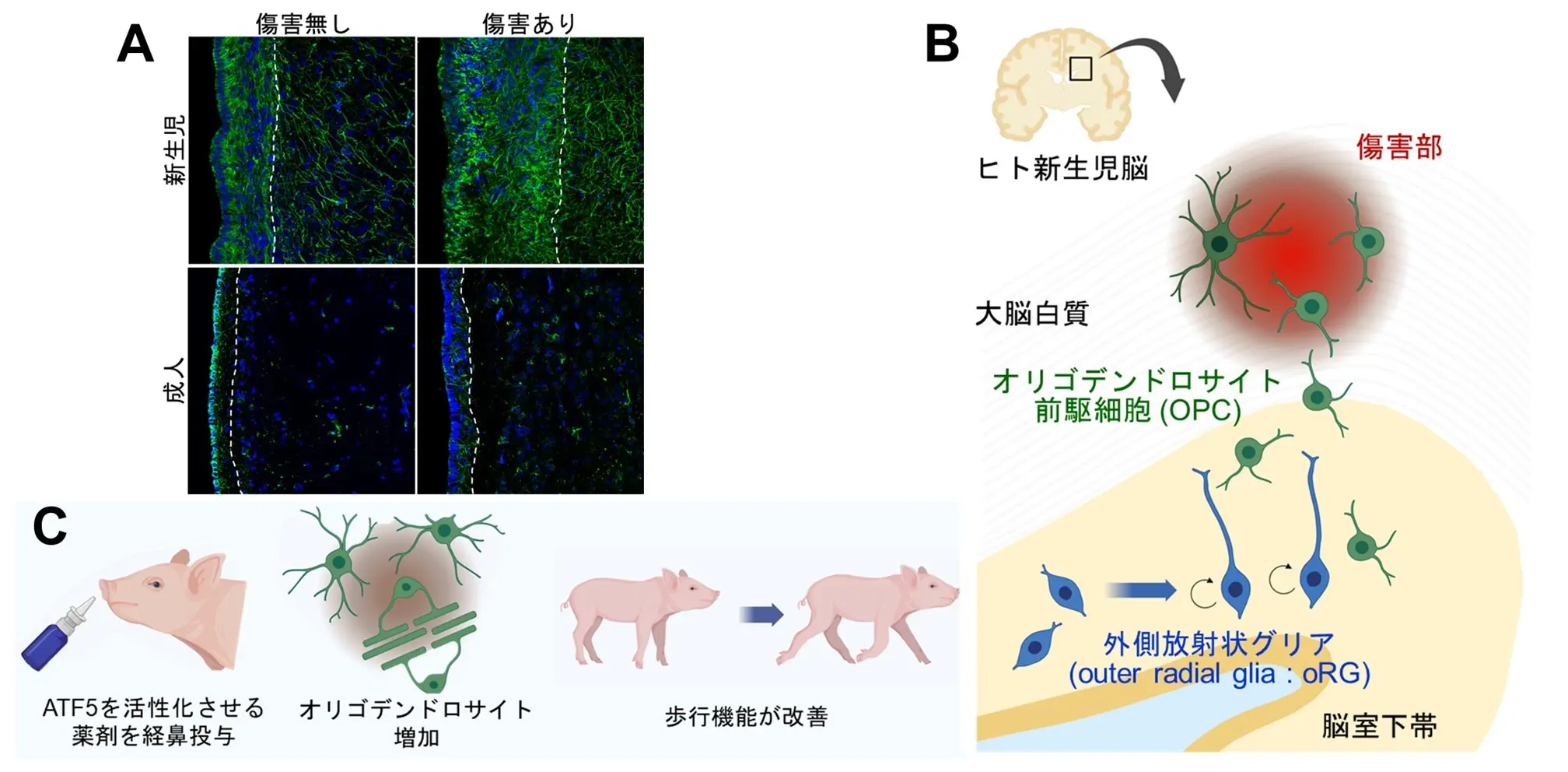
図:本研究の成果
? 2025 Jinnou et al. Originally published in Cell Reports Medicine
DOI番号:10.1016/j.xcrm.2025.101986
A.ヒト脳室下帯の解析。新生児の脳室下帯は成人より大きく、傷害で拡大する。
B.新生児脳障害後に脳室下帯の外側放射状グリア細胞の増殖能力が増強され、産生されたオリゴデンドロサイト前駆細胞が白質傷害部へ移動して一部が分化する。
C.脳障害を持つ新生仔ブタへATF5シグナルを活性させる薬剤(サルブリナール)を経鼻投与すると、白質傷害部のオリゴデンドロサイトが増加して白質が再生され、歩行機能が改善する。
用語解説
注1 神経幹細胞:自己複製能と多分化能を併せもった未分化な細胞。中枢神経系を構成するニューロン(神経細胞)およびグリア細胞(アストロサイト、オリゴデンドロサイト)を産生する。
注2 外側放射状グリア:脳室下帯の外側に存在する神経幹細胞。マウスでは認められず、ヒトや霊長類、ブタなど大脳にしわを持つ動物種に特徴的な細胞。胎児期では多数のニューロン?グリア細胞を産生して脳の拡大や複雑な脳構造の形成に寄与していることが知られている。
注3 オリゴデンドロサイト前駆細胞:オリゴデンドロサイトへ分化する前駆細胞。オリゴデンドロサイトは神経伝導速度を高める髄鞘を形成する。髄鞘で包まれた神経線維の束が白質となる。
注4 拡散テンソル画像解析:MRI画像を用いて脳内の神経線維の走行を可視化する解析法。
注2 外側放射状グリア:脳室下帯の外側に存在する神経幹細胞。マウスでは認められず、ヒトや霊長類、ブタなど大脳にしわを持つ動物種に特徴的な細胞。胎児期では多数のニューロン?グリア細胞を産生して脳の拡大や複雑な脳構造の形成に寄与していることが知られている。
注3 オリゴデンドロサイト前駆細胞:オリゴデンドロサイトへ分化する前駆細胞。オリゴデンドロサイトは神経伝導速度を高める髄鞘を形成する。髄鞘で包まれた神経線維の束が白質となる。
注4 拡散テンソル画像解析:MRI画像を用いて脳内の神経線維の走行を可視化する解析法。
研究助成
本研究は、JSPS科研費(JP22K15902、JP24K11026、JP24K22003、JP24H02016、JP20H05700、JP23K05770)、JSPS研究拠点形成事業(JPJSCCA20230007)、日本医療研究開発機構(AMED)の革新的先端研究開発支援事業の研究課題「ニューロン移動による傷害脳の適応?修復機構とその操作技術」(研究開発代表者:澤本和延)、武田科学振興財団、日東学術振興財団などによる助成を受けて行われました。
掲載情報
【論文タイトル】
Outer radial glia promotes white matter regeneration after neonatal brain injury
「外側放射状グリアは新生児脳障害後の白質再生を促進する」
【著者】
神農 英雄1,2, Lauren M. Rosko2, Satoshi Yamashita2, Soichiro Henmi2, Jaya Prasad2, Van K. Lam2, Artur Agaronyan3, Tsang-Wei Tu3, Yuka Imamura4, 久保山和哉5, 澤本和延5, Kazue Hashimoto-Torii2,6, Nobuyuki Ishibashi2,6*, Vittorio Gallo2,6,7,8*
1.365体育投注大学院医学研究科 新生児?小児医学分野
2.Children's National Research Institute, Children's National Hospital
3.Howard University
4.Pennsylvania State University College of Medicine
5.365体育投注大学院医学研究科 脳神経科学研究所 神経発達?再生医学
6.George Washington University School of Medicine and Health Sciences
7.Seattle Children’s Hospital
8.University of Washington
*責任著者
【掲載学術誌】
学術誌名 「Cell Reports Medicine(セルリポーツメディシン)」
DOI番号:10.1016/j.xcrm.2025.101986
Outer radial glia promotes white matter regeneration after neonatal brain injury
「外側放射状グリアは新生児脳障害後の白質再生を促進する」
【著者】
神農 英雄1,2, Lauren M. Rosko2, Satoshi Yamashita2, Soichiro Henmi2, Jaya Prasad2, Van K. Lam2, Artur Agaronyan3, Tsang-Wei Tu3, Yuka Imamura4, 久保山和哉5, 澤本和延5, Kazue Hashimoto-Torii2,6, Nobuyuki Ishibashi2,6*, Vittorio Gallo2,6,7,8*
1.365体育投注大学院医学研究科 新生児?小児医学分野
2.Children's National Research Institute, Children's National Hospital
3.Howard University
4.Pennsylvania State University College of Medicine
5.365体育投注大学院医学研究科 脳神経科学研究所 神経発達?再生医学
6.George Washington University School of Medicine and Health Sciences
7.Seattle Children’s Hospital
8.University of Washington
*責任著者
【掲載学術誌】
学術誌名 「Cell Reports Medicine(セルリポーツメディシン)」
DOI番号:10.1016/j.xcrm.2025.101986

